Līdz šim smadzeņu traumas (CMT) ir viens no visbiežāk sastopamajiem neiroloģiskās patoloģijas veidiem un ir nozīmīga medicīniska un sociāli ekonomiska problēma visiem iedzīvotāju segmentiem.
Saturs
Attīstītajās valstīs pastāv stabils neirotraumimamisma pieaugums. Tātad Eiropas valstīs 150 ir reģistrēta katru gadu–300 chmt gadījumi uz 100 tūkstošiem. Populācija. ASV, tikai 2003. Atzīmēja vairāk nekā 1,5 miljonus cmt. Krievijā šis skaitlis sasniedz 4 gadījumus uz 1000. Cilvēks. Svarīgākā problēma medicīnisko ziņā ir tāda, ka ievērojams skaits upuru pēc tam izstrādā tā sauktās sekas atlikta CMT, kas bieži interpretē pēc traumatiskā encefalopātija. Starp visbiežāk sastopamajiem sindromiem, kas nosaka sociālo mājsaimniecību pielāgošanās līmeni un pacientu dzīves kvalitāti, ir intelektuālie unikālie pārkāpumi. Pēc traumatiski kognitīvie traucējumi ir izolēti 29,4% no visiem pacientiem ar CHMT sekām, un kopā ar citiem sindromiem — y 35,7%. Kopumā starp atlikušo CMT kognitīvo traucējumu sekām, jo sindroms ir atrodams 65.1% gadījumu.
Pēc traumatisku kognitīvo traucējumu attīstības patoģenēze ir ļoti sarežģīta un daudzveidīga. Kā galvenie faktori, kas var novest pie kognitīvā deficīta veidošanās akūtā periodā, mēs uzskatām gan tiešus mehāniskus bojājumus smadzeņu audiem, gan dažu patofizioloģisko procesu, kas izriet no cht, piemēram, smadzeņu pietūkuma pietūkums, \ t šķidruma, hemodinamikas un Dr. Tajā pašā laikā ir zināms, ka attiecībā uz intelektuālā ēdiena funkciju traucējumu gadījumiem, ilgs laiks tiek saglabāts vai ir noturīgs raksturs. Citos pacientiem tie parādās tālā kaitējuma periodā un ir atšķirīga tendence virzīties uz progresēšanu. Šādu pārkāpumu gadījuma mehānisms joprojām nav pētīts tiesiskās aizsardzības līdzekļos. Iegūtie dati liecina, ka patoloģiskie faktori skar nervu šūnu akūtā periodā, veicina neironu bioķīmisko maiņu kaskādes rašanos, kas noved pie dēmstrofisko procesu attīstību un samazina sinstrofisko pārraides efektivitāti.
Galu galā, ir pārkāpts informācijas izplatīšanas procesu neironu tīklos, kas tiek uzskatīts par vienu no galvenajiem aspektiem, veidojot kognitīvo pārkāpumu. Vairāki pētnieki atzīmē dažu līdzību patogenētisko mehānismu attīstībai kognitīvo traucējumu CMT un asinsvadu smadzeņu bojājumiem. Turklāt iespējamā smadzeņu traumu loma tiek parādīta kā neirodeģeneratīvo slimību palaišana, jo īpaši Alcheimera slimība. Pašlaik vairāki patofizioloģiskie procesi ir nozīmīga loma pēc traumatisku kognitīvo traucējumu veidošanā.
Viens no šiem procesiem ir attīstība «Glutamāts Exaitotoxicity». Fizioloģiskajos apstākļos glutamāts darbojas kā viens no svarīgākajiem aizraujošajiem centrālās nervu sistēmas aizraujošajiem starpniekiem, piedaloties neironu plastmasas procesu īstenošanā un smadzeņu integrējošās funkcijas. Nozīmīgs daudzums glutamanthergic receptoru novēro smadzeņu garozā un hipokampu. Tajā pašā laikā ar patoloģiju, tiek novērotas pārmērīgas glutamāta emisijas, kas šajos apstākļos ir toksiska iedarbība uz neironu struktūrām, kas veicina glutamāta-kalcija kaskādes reakciju aktivizēšanu, kas izraisa nekontrolētu intracelulārā kalcija koncentrācijas palielināšanos , kam ir negatīva ietekme uz šūnu energoapgādi. Tiek parādīts, ka saskaņā ar išēmijas apstākļos audos ir ievērojams brīvo radikāļu veidošanās līmenis, kas arī veicina kalcija intracelulāro uzkrāšanos.
Smadzenes ir ļoti jutīgas pret brīvo radikāļu darbību. Oksidantu sistēmu pārsvarā antioksidantā, tā sauktā oksidētā stresa veidošanās apstākļos. Šādā gadījumā tiek aktivizēta fosfolipāzes hidrolīze, un šūnu membrānas ir degradācija, tostarp mitohondriju. Jaunās traucējumu novēršana ir priekšnoteikums veiksmīgai pacientu vadībai ar post-traumatiskiem kognitīvajiem traucējumiem. Ar šīm pozīcijām, tas ir lietderīgi iecelt šādu narkotiku kā Noopept ar šādām īpašībām. Noopept — N-fenil-acetil-l-prolyglycine etilesteris — Jauns iekšzemes sākotnējais dipeptīds, kas izveidots farmakoloģijā. Iebildums.Iebildums.Zasakova ramne. Saskaņā ar datiem, kas iegūti eksperimentālo pētījumu gaitā, Nopept ir nootropiskas un neiroprotektīvas īpašības. Zāles tās strukturālajās iezīmēs ir līdzīgs Piracetam un VasoPressin. Šīs narkotikas attīstība tika veikta kā daļa no esošās idejas, ka dažiem regulējošiem peptīdiem ir būtiska ietekme uz atmiņas un apmācības mehānismiem.
Noopept prasības pamatojums ir hipotēze, ka šīs Piracetamas grupas bāzes zāles ir peptīda liganda analogs konkrētiem nootropiskiem receptoriem, līdzīgi tās īpašībām ar vasopressin metabolītiem. Noopreps ir izdevīgs no vasopressin, jo tas spēj parādīt darbību ar sistēmisku, tostarp iekšķīgu lietošanu. Studiju laikā tika parādīts zāļu augstais biopieejamība smadzeņu audiem, kā arī tās zemā toksicitāte. Pētījums eksperimentā ar laboratorijas dzīvniekiem ļāva noteikt, ka narkotiku devu lietošana no 2 līdz 20 reizes lielāks nekā nootropisks, nerada kaitējumu iekšējiem orgāniem, nav būtisku hematoloģisko un bioķīmisko rādītāju pārkāpumu. Veicot vairākus klīniskos pētījumus, tiek parādīta arī liela zāļu drošība un tā laba panesamība. Pētījuma gaitā tika konstatēts, ka Noopept ir visaptverošs rīcības mehānisms.
Pirmkārt, tas ir nootropisks efekts, kas saistīts ar to, ka viens no aktīvajiem metabolītiem Noopept ir cikloprolglycine, kas savā struktūrā ir līdzīgs endogēnai cikliskajam Dippotide, kam ir anti-inficic aktivitāte.
Otrkārt, Noopept spēj palielināt smadzeņu audu stabilitāti, lai kaitētu triecieniem, piemēram, traumas, hipoksisku, elektronisko un toksisku bojājumu, kas raksturo šīs narkotikas neiroprotektīvo ietekmi. Treškārt, ir pierādīts, ka noopept, lai novērstu glutamāta toksisko koncentrāciju un neironu skābekļa nāves aktīvās formas smadzeņu garozā un smadzeņu garozā. Turklāt eksperiments atklāja spēju samazināt b-amiloidu toksisko iedarbību, uzlabo anti-mylide antivielu ražošanu, modulēt holīnerģisko receptoru darbību, kā arī stimulē neirotrofisko faktoru izpausmi (BDNF un NGF) smadzeņu garozas un hipokamps.
Pēc traumatisko kognitīvo pārkāpumu problēmas atbilstība Noopept lietošanas derīgumam, ņemot vērā pieteikuma punktu klātbūtni neiroķīmiskā līmenī CHT sekas, kā arī sākotnējo, tostarp eksperimentālo un Šā pētījuma iemesls bija narkotiku klīniskā efektivitāte.
Pētījuma mērķis bija novērtēt efektivitāti, kā arī narkotiku lietošanas drošību pacientiem ar vieglām pēc traumatiskiem kognitīvajiem traucējumiem. Pētījums tika veikts ar speciāli izstrādātu protokolu un ievērojis visas atbilstošas klīniskās prakses (GCP) prasības, kas pieņemts Krievijas Federācijā. Pētījumā tika iekļauti pacienti, kas atbilst kritērijiem iekļaušanai pēc obligātās informētas piekrišanas parakstīšanas.
30 pacienti vecumā 19 piedalījās pētījumā–66 gadus vecs (vidējais vecums 33±10,3 gadi), kas cieta no chht (satricinājums vai traumas smadzeņu gaismas pakāpes) vismaz pirms 6 mēnešiem un ar šo valsti saistīto intelektuālā ēdināšanas funkciju pārtraukšanu, kas atbilst mērenas kognitīvo traucējumu sindroma kritērijiem. Visi pacienti atbilst kritērijiem attiecībā uz mērenu kognitīvo pārkāpumu sindromu, un to kognitīvie traucējumi sākotnēji tika novērtēti 25 vai vairāk punktos par mini garīgās valsts pārbaudes skalu (MMSE).
Izņēmumi kritēriji no pētījuma bija: vienlaicīgu smago vai nestabilu somatisko slimību klātbūtne, kas apdraud pacienta dzīvi, klīniski nozīmīgu citu klātbūtni (izņemot mērenu kognitīvo pārkāpumu sindromu ar CHF sekām) neiroloģiskiem vai garīgiem traucējumiem, \ t rupja motora vai sensoro defektu vai citu traucējumu klātbūtne, kas apgrūtināja neiropsiholoģisku pētījumu vai citus protokolā paredzētos pētījumus, insulta vai nepārklājošā encefalopātijas III posmu, vienlaicīgu terapiju ar citu vazoaktīvo, \ t vielmaiņas vai psihotropās zāles ar pierādītu kognitīvo stimulējošo efektu, neiecietību uz narkotiku pētījuma, grūtniecības un laktācijas periodā.
Veicot darbu, lai objektīvi iebilstat ar iegūtajiem datiem
Šādas metodes:
1) neiroloģiskā stāvokļa novērtējums;
2) īss garīgās statusa skala — Mmīns;
3) Hamilton svari, lai novērtētu depresiju;
4) Testa akumulators frontālās disfunkcijai — Frontālās vērtēšanas akumulators (FAB);
5) skatīties zīmēšanas tests;
6) 10 vārdi;
7) izmēģinājuma schulte;
8) Vērtēšanas apjoms vispārējā klīniskā iespaidā par izmaiņām — Ārstam’S intervija balstīta iespaids par izmaiņām plus (cibic plus);
9) Neiroviasualizācijas metodes: dators vai magnētiskā rezonanses tomogrāfija.
Vispārējās klīniskās pieredzes mēroga novērtējums, kas paredzēts pacienta stāvokļa novērtēšanai līdz terapijai un izmaiņu smaguma novērtēšanai ārstēšanas fonā. Ārstējošais ārsts pirms terapijas sākuma novērtēja pacienta stāvokli, pamatojoties uz analīzi par traucējumiem 7-punktu skalā, novērtējot slimības klīnisko priekšstatu, uzraudzīt pacientu, stāvokli garīgās sfēras Pacients, uzvedība, sociālo iekšzemes funkciju stāvoklis.
Pētījuma sākumā tika veikta skrīninga vizīte, par kuru pacienta atbilstību noteica iekļaušanas kritēriji. Tad, ja pacienta atbilstības, protokols parakstīja informētu piekrišanu. Šī vizīte arī novērtēja elektrokardiogrammu, laboratorijas un neirovalizācijas pētījumu metožu rezultātus. Pēc tam tika novērtēts neiroloģiskais stāvoklis, tika veikta pamata neiropsiholoģiskā pārbaude, lai noteiktu kognitīvo funkciju sākotnējo līmeni.
Sākot ar nākamo skrīninga vizītes dienu, pacienti 60 dienu laikā saņēma Noopept 10 mg 2 reizes dienā 60 dienas. Nākotnē tika veikta terapijas efektivitātes novērtēšana 30. un 60. ārstēšanas dienās. Pasākumu plāns ir norādīts tabulā.
Mūsu pētījumā vidējais periods pēc cieta kaitējuma bija 7±3,8 gadi. Visi 30 pacienti, kuri ir ieradušies pētījumā, sākotnēji bija vieglas pārkāpumi par vispārējo klīnisko iespaidu par izmaiņām (CIBIC Plus). Pārbaudes vizītes laikā visi pārbaudītie pacienti iepazīstināja ar sūdzībām par atmiņas samazināšanu, uzmanības koncentrāciju, samazinot ikdienas aktivitāšu veikšanas efektivitāti, vispārējo vājumu, palielinot nogurumu. Turklāt daži no pacientiem iesniedza citas sūdzības: uz galvassāpēm (43,3%), grūtības plānot dažādas darbības (40%), miega traucējumi (26,7%), garastāvokļa nestabilitāte (23,3%). Bruto pārkāpumu neiroloģiskā izmeklēšana netika konstatēta. 53,3% pacientu bija izkaisīti simptomi izolētu mikrosimptu formā, 13,3% — Gaismas koordinatora pārkāpumi. Tajā pašā skaitā novēroto divpusējo patoloģisko plastmasas refleksu (Rossolimo, Vartenberg). Visiem pacientiem bija astēna sindroma pazīmes. 53,3% ir novērojuši veģetatīvās un asinsvadu nestabilitātes pazīmes.
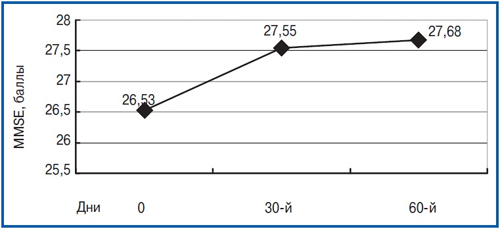
Dinamikā veikto pacientu kognitīvo funkciju izpēte parādīja, ka pēc MMSE mēroga rezultātiem ticamas atšķirības ar sākotnējo līmeni tika uzrādītas 30 dienas pēc ārstēšanas sākuma. Jo īpaši pirms narkotiku uzņemšanas vidējais rezultāts bija 26.5±0,94; 1 mēnesis no terapijas sākuma — 27.6±0,99 punkti (p<0,01). Tajā pašā laikā 60 dienas no terapijas sākuma vidējais rādītājs šajā mērogā bija 27.7±1.09, kas raksturoja tālāku uzticamu uzlabojumu trūkumu (p>0,05) un tika parādīta tikai tendence samazināt kognitīvās traucējumus. Neiropsiholoģisko rādītāju dinamika uz MMSE skalā ir parādīta rīsiem. viens.
1. attēls
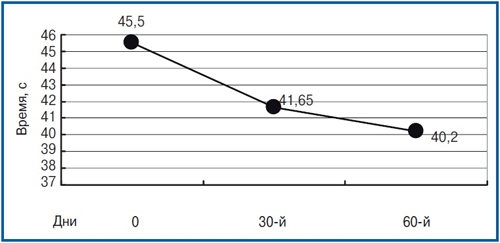
Interesanti bija fakts, ka struktūrā MMSE skala, visnozīmīgākais uzlabojums rādītājos tika iegūta ar Subshkalale «Uzmanība», raksturojot zināmā mērā stāvoklis neirodinamisko procesu cieš no TBMC (P<0,01), kā arī Subshkalale «atmiņa» (R<0.05). Uz akumulatora skalas testiem, lai novērtētu frontālo disfunkciju Fab uzticamu atšķirību pār novērošanas periodu dinamikā nebija pieejama (sākotnējā vizītē — 15.9±0,78 punkti, 60 dienas vēlāk — 16.8±0,87, p = 0,27). Pulksteņa zīmēšanas testa tests ar 10 punktu aprēķinu par avota apmeklējumu parasti tiek novērtēts 9–10 punkti un pret būtisku izmaiņu ārstēšanu netika veikta. Protams, dati, kas iegūti, pamatojoties uz novērtējumu par izlases rezultātu šulte, kas tika veikta uz visiem 3 apmeklējumiem. Visaptverošs aprēķinātais paraugs, izmantojot 5 secīgi iesniegtos pacientu tabulas, kas visvairāk pilnībā ļauj raksturot šādas neirodinamiskās izmaiņas kā uzmanības koncentrācijas pasliktināšanos, palielinot garīgo procesu izsīkšanu un nestabilitātes uzmanību. Šīs izmaiņas zināmā mērā raksturoja lielākā daļa pacientu skrīninga apmeklējumos. Vidējais pārbaudes laiks katram no pieciem prezentācijām pirmajā vizītē bija 45,5±6.24 S. Pēc 2 mēnešiem pēc terapijas uzsākšanas laiks samazinājās līdz 40.2±5.20 S, kas raksturoja ievērojamu uzmanības uzlabošanu uzmanības koncentrācijā (p<0.05). Schulte izlases laika dinamika ir parādīta rīsiem. 2.
2. attēls
Kā redzams no grafika rīsiem. 2, pacientiem 30 dienu laikā pēc terapijas sākuma parādīja nozīmīgāko laiku, kas pavadīts uz paraugu izpildei iztērētajam laikam. Pozitīvas dinamikas atpazīšana notika arī 2. mēneša laikā narkotiku otrajā mēnesī, un to raksturoja vēl izteiktāka testa laika samazināšanās ar mazāk nozīmīgu uzlabošanas stabilizāciju nekā MMSE skalā.
Vispārējās klīniskās pieredzes mēroga novērtējums, kas paredzēts pacienta stāvokļa novērtēšanai līdz terapijai un izmaiņu smaguma novērtēšanai ārstēšanas fonā. Ārstējošais ārsts pirms terapijas sākuma novērtēja pacienta stāvokli, pamatojoties uz analīzi par traucējumiem 7-punktu skalā, novērtējot slimības klīnisko priekšstatu, uzraudzīt pacientu, stāvokli garīgās sfēras Pacients, uzvedība, sociālo iekšzemes funkciju stāvoklis.
Pētījuma sākumā tika veikta skrīninga vizīte, par kuru pacienta atbilstību noteica iekļaušanas kritēriji. Tad, ja pacienta atbilstības, protokols parakstīja informētu piekrišanu. Šī vizīte arī novērtēja elektrokardiogrammu, laboratorijas un neirovalizācijas pētījumu metožu rezultātus. Pēc tam tika novērtēts neiroloģiskais stāvoklis, tika veikta pamata neiropsiholoģiskā pārbaude, lai noteiktu kognitīvo funkciju sākotnējo līmeni.
Sākot ar nākamo skrīninga vizītes dienu, pacienti 60 dienu laikā saņēma Noopept 10 mg 2 reizes dienā 60 dienas. Nākotnē tika veikta terapijas efektivitātes novērtēšana 30. un 60. ārstēšanas dienās. Pasākumu plāns ir norādīts tabulā.
| Pētniecības metodes | I | II | III |
| Fons | 30. diena | 60. diena | |
| Garīgās statusa novērtējuma kolekcija (MMSE) | V | V | V |
| Frontālās disfunkcijas (FAB) novērtējums | V | V | |
| Testa zīmēšanas stundas 10 – Pakalns novērtējums | V | V | |
| Vispārējā klīniskā iespaids (CGI) | V | V | |
| Test 10 vārdi | V | V | |
| Izlases schulte | V | V | V |
| Hamilton mērogs | V | ||
| Nevēlamo parādību un blakusparādību novērtējums | V | V |
3. attēls
Mūsu pētījumā vidējais periods pēc cieta kaitējuma bija 7±3,8 gadi. Visi 30 pacienti, kuri ir ieradušies pētījumā, sākotnēji bija vieglas pārkāpumi par vispārējo klīnisko iespaidu par izmaiņām (CIBIC Plus). Pārbaudes vizītes laikā visi pārbaudītie pacienti iepazīstināja ar sūdzībām par atmiņas samazināšanu, uzmanības koncentrāciju, samazinot ikdienas aktivitāšu veikšanas efektivitāti, vispārējo vājumu, palielinot nogurumu. Turklāt daži no pacientiem iesniedza citas sūdzības: uz galvassāpēm (43,3%), grūtības plānot dažādas darbības (40%), miega traucējumi (26,7%), garastāvokļa nestabilitāte (23,3%). Bruto pārkāpumu neiroloģiskā izmeklēšana netika konstatēta. 53,3% pacientu bija izkaisīti simptomi izolētu mikrosimptu formā, 13,3% — Gaismas koordinatora pārkāpumi. Tajā pašā skaitā novēroto divpusējo patoloģisko plastmasas refleksu (Rossolimo, Vartenberg). Visiem pacientiem bija astēna sindroma pazīmes. 53,3% ir novērojuši veģetatīvās un asinsvadu nestabilitātes pazīmes.
Dinamikā veikto pacientu kognitīvo funkciju izpēte parādīja, ka pēc MMSE mēroga rezultātiem ticamas atšķirības ar sākotnējo līmeni tika uzrādītas 30 dienas pēc ārstēšanas sākuma. Jo īpaši pirms narkotiku uzņemšanas vidējais rezultāts bija 26.5±0,94; 1 mēnesis no terapijas sākuma — 27.6±0,99 punkti (p<0,01). Tajā pašā laikā 60 dienas no terapijas sākuma vidējais rādītājs šajā mērogā bija 27.7±1.09, kas raksturoja tālāku uzticamu uzlabojumu trūkumu (p>0,05) un tika parādīta tikai tendence samazināt kognitīvās traucējumus. Neiropsiholoģisko rādītāju dinamika uz MMSE skalā ir parādīta rīsiem. viens. Interesanti bija fakts, ka struktūrā MMSE skala, visnozīmīgākais uzlabojums rādītājos tika iegūta ar Subshkalale «Uzmanība», raksturojot zināmā mērā stāvoklis neirodinamisko procesu cieš no TBMC (P<0,01), kā arī Subshkalale «atmiņa» (R<0.05). Uz akumulatora skalas testiem, lai novērtētu frontālo disfunkciju Fab uzticamu atšķirību pār novērošanas periodu dinamikā nebija pieejama (sākotnējā vizītē — 15.9±0,78 punkti, 60 dienas vēlāk — 16.8±0,87, p = 0,27). Pulksteņa zīmēšanas testa tests ar 10 punktu aprēķinu par avota apmeklējumu parasti tiek novērtēts 9–10 punkti un pret būtisku izmaiņu ārstēšanu netika veikta.
Protams, dati, kas iegūti, pamatojoties uz novērtējumu par izlases rezultātu šulte, kas tika veikta uz visiem 3 apmeklējumiem. Visaptverošs aprēķinātais paraugs, izmantojot 5 secīgi iesniegtos pacientu tabulas, kas visvairāk pilnībā ļauj raksturot šādas neirodinamiskās izmaiņas kā uzmanības koncentrācijas pasliktināšanos, palielinot garīgo procesu izsīkšanu un nestabilitātes uzmanību. Šīs izmaiņas zināmā mērā raksturoja lielākā daļa pacientu skrīninga apmeklējumos. Vidējais pārbaudes laiks katram no pieciem prezentācijām pirmajā vizītē bija 45,5±6.24 S. Pēc 2 mēnešiem pēc terapijas uzsākšanas laiks samazinājās līdz 40.2±5.20 S, kas raksturoja ievērojamu uzmanības uzlabošanu uzmanības koncentrācijā (p<0.05). Schulte izlases laika dinamika ir parādīta rīsiem. 2. Kā redzams no grafika rīsiem. 2, pacientiem 30 dienu laikā pēc terapijas sākuma parādīja nozīmīgāko laiku, kas pavadīts uz paraugu izpildei iztērētajam laikam. Pozitīvas dinamikas atpazīšana notika arī 2. mēneša laikā narkotiku otrajā mēnesī, un to raksturoja vēl izteiktāka testa laika samazināšanās ar mazāk nozīmīgu uzlabošanas stabilizāciju nekā MMSE skalā.